| Titel: | Beschreibung eines Apparats zum Auffinden mehrerer Säuren; von Pisani. |
| Fundstelle: | Band 163, Jahrgang 1862, Nr. XIV., S. 62 |
| Download: | XML |
XIV.
Beschreibung eines Apparats zum Auffinden
mehrerer Säuren; von Pisani.
Aus den Annales des
mines, 5me série, 1861, t. XIX p. 477.
Mit einer Abbildung auf Tab. I.
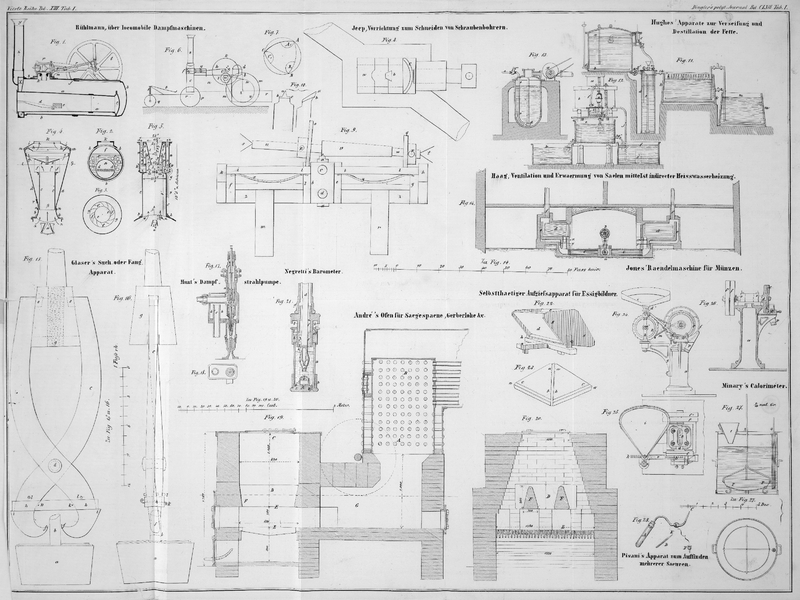
Pisani's Apparat zum Auffinden mehrerer Säuren.
Dieser kleine, in Fig. 28 abgebildete Apparat ist sehr bequem, wenn man Proben im Kleinen
macht, und eignet sich daher besonders für Untersuchungen mit dem Löthrohr.
Er besteht aus einer 6 bis 8 Centimeter langen Glasröhre A, an der man mittelst eines Pfropfes die Kugelröhre B befestigt, welche bei C
schwach ausgezogen ist. Nur zum Aufsuchen der Oxalsäure verbindet man mit dem Theil
C mittelst einer Kautschukröhre den Ansatz D, worin sich Kalihydrat in Stücken zwischen zwei
Baumwollbällchen befindet. Ein kleiner Trichter F dient
zum Eingießen der Reagentien, welche man in der Kugel B
anwendet.
Mittelst dieses Apparats kann man folgende Säuren erkennen:
Kohlensaure Salze. – Man bringt in die Kugel
einige Tropfen Kalkwasser und in die Röhre die mit zweifach-schwefelsaurem
Kali gemengte Substanz. Man erhitzt und das Kalkwasser wird getrübt. Wenn man ein
zweifach- oder anderthalb-kohlensaures Alkali hat, so erhitzt man die
Substanz für sich allein. Es ist sogar leicht, gewisse kohlensaure Salze von
einander zu unterscheiden; so entbindet die kohlensaure Magnesia sehr leicht
Kohlensäure beim Erhitzen mit einer gewöhnlichen Gaslampe, während kohlensaurer
Baryt, Strontian und Kalk, sowie der Dolomit keine entbinden; erst nachdem sie sehr
stark und lange Zeit erhitzt worden sind, geben die beiden letzteren ein wenig
Kohlensäure ab. Der Spatheisenstein und die anderen kohlensauren Metalloxyde liefern
hingegen sehr leicht Kohlensäure.
Oxalsäure Salze. – Bekanntlich geben die
oxalsauren Salze, mit Schwefelsäure erhitzt, Kohlenoxydgas und Kohlensäure. In
meinem Apparat erhitze ich die Substanz mit zweifach-schwefelsaurem Kali,
nachdem ich Kalkwasser in die Kugel gegossen und an dem Theil C den (Kalistückchen enthaltenden) Ansatz D
angebracht habe; das Kalkwasser trübt sich alsdann, und man entzündet das Kohlenoxyd
am ausgezogenen Ende des Ansatzes. Letzterer ist nothwendig, um die Antheile von
Kohlensäure zurückzuhalten, welche dem Kohlenoxyd beigemischt bleiben.
Salpetersaure Salze. – Die Substanz wird mit
zweifach-schwefelsaurem Kali erhitzt, und man gießt in die Kugel einige
Tropfen schwefelsaures Eisenoxydul, welches sich unter dem Einfluß der salpetrigen
Dämpfe rasch bräunt.
Cyanverbindungen. – Um das Cyan zu erkennen,
bringt man in die Kugel eine Aetzkalilösung und in die Röhre das Gemenge der
Substanz mit zweifach-schwefelsaurem Kali: man erhitzt und es bildet sich so
Cyankalium. Man gießt den Inhalt der Kugel in ein Uhrglas, welches mit Salzsäure
angesäuertes schwefelsaures Eisenoxydul-Oxyd enthält, und bekommt so
Berlinerblau.
Chloride. – Man vermengt die Substanz mit
zweifach-chromsaurem Kali, und erhitzt dieses Gemenge mit concentrirter
Schwefelsäure: in der Kugel verdichtet sich chromsaures Chromchlorid, welches in
Ammoniak gegossen eine gelbe Auflösung von chromsaurem Amoniak gibt. Diese Reaction
ist auf die meisten löslichen Chloride anwendbar.
Gemenge von Chloriden und Bromiden. – Man verfährt
wie vorher, und constatirt so die Gegenwart des Chlors; um das Brom aufzufinden,
stellt man einen besonderen Versuch an.
Bromide. – Man erhitzt dieselben mit
zweifach-schwefelsaurem Kali; es entbindet sich Brom, welches sich im krummen
Theil der Kugelröhren oder in der Kugel selbst verdichtet. Wenn zugleich sehr wenig
Jod vorhanden ist, wie im käuflichen Bromkalium, so bemerkt man in der Röhre seinen
violetten Dampf. Fast alle löslichen Bromide geben diese Bromreaction mit dem
zweifach-schwefelsauren Kali.
Jodide. – Das frei gemachte Jod erkennt man leicht
an der Farbe seines Dampfes.
Tafeln