| Titel: | Ueber die Bestimmung des Kohlenstoffs im Stahl; von W. Weyl. |
| Fundstelle: | Band 179, Jahrgang 1866, Nr. LXXIII., S. 297 |
| Download: | XML |
LXXIII.
Ueber die Bestimmung des Kohlenstoffs im Stahl;
von W. Weyl.
Aus Poggendorff's Annalen der Physik und Chemie, 1865, Bd. CXXVI S.
617.
Mit einer Abbildung auf Tab. VI.
Weyl, über Bestimmung des Kohlenstoffs im Stahl.
Schon vor mehreren Jahren veröffentlichte ich ein Verfahren zur Bestimmung des
Kohlenstoffes in EisenPolytechn. Journal Bd. CLXIII S.
120. welches im Wesentlichen darin besteht, daß das Eisen, auf elektrolytischem
Wege in Lösung gebracht, seine ihm äquivalente Menge Wasserstoff an dem
gegenüberstehenden negativen Pol abscheidet, während der Kohlenstoff des als
positiver Pol functionirenden Eisenstückes nach der Lösung desselben als
Pseudomorphose zurückbleibt und zu Kohlensäure verbrannt genau bestimmt werden
kann.
Daß dieses Verfahren bei Spiegeleisen zu sicheren Resultaten führt, haben die von mir
angestellten Versuche außer Zweifel gesetzt, und ließ sich von vorn herein schon
erwarten, daß der Anwendung desselben auf graues Eisen, Schmiedeeisen und Stahl
nichts entgegenstehe; dieß doch selbstverständlich nur so lange als Kohlenstoff und
Wasserstoff im status nascens nicht in unmittelbaren
Contact zu einander treten. Diese conditio sine qua non
scheint einem Hrn. Reimann freilich entgangen zu seyn und
daher das vergebliche Abmühen desselben, den Kohlenstoff auf diese Weise im Stahl zu
bestimmen; denn es scheidet sich bei der Elektrolyse des Stahls der Kohlenstoff in
so äußerst fein vertheiltem Zustande aus, daß derselbe nicht etwa als fest
zusammenhängende Masse wie bei dem Spiegeleisen zurückbleibt, sondern sich ablöst
von dem positiven Pol und, der mechanisch schiebenden Wirkung des Stromes nach dem
negativen Pole hin folgend, an diesem theilweise sich absetzt, theilweise mit dem
Wasserstoff daselbst zusammentritt und als Kohlenwasserstoff entweicht.
Die hier störend auftretenden Folgen der äußerst merkwürdigen mechanischen Wirkung
des Stromes (die vor mehreren Jahren von Quincke näher
studirt wurde) läßt in einfachster Weise sich beseitigen durch eine zwischen die
Pole geschobene poröse Scheidewand, wie thierische Blase, der gewiß auch und sehr
zweckmäßig Pergament-Papier sich substituiren läßt. Zwar beobachtet man auch
hier, daß nach mehreren Stunden ein schwarzer Körper auf der negativen Elektrode
sich absetzt, der jedoch in Salzsäure löslich als Eisen sich erweist, herrührend von
dem Eisenchlorür, welches die Scheidewand selbstverständlich durchdrungen, sich elektrolysirt mit
der Salzsäure und, wie diese an dem negativen Pole Wasserstoff, so seinerseits Eisen
abgeschieden hat.
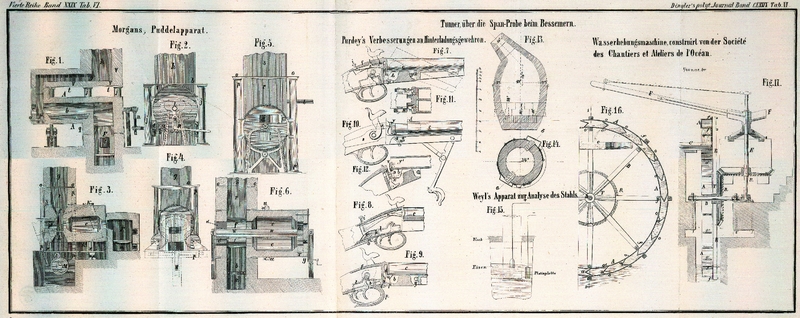
Die bei diesem Versuche von mir getroffene Anordnung besteht, wie aus der Skizze Fig. 15
ersichtlich, aus einem Becherglase zur Hälfte gefüllt mit verdünnter Salzsäure, in
die ein Glascylinder sich einsenkt, der unten durch Blase geschlossen und bis auf
eine mit der umgebenden Flüssigkeit gleiche Höhe ebenfalls mit verdünnter Säure
gefüllt ist. Der Cylinder enthält die positive Elektrode, der Raum zwischen ihm und
dem Becherglase die negative. Im Uebrigen ist das inne zu haltende Verfahren
vollkommen identisch mit dem bereits bekannten.
Ich schließe hieran noch die Mittheilung einer gelegentlich von mir gemachten
Beobachtung, die es, wie ich dafürhalte, gleichfalls ermöglicht, den Kohlenstoff im
Eisen sicher zu bestimmen. Es läßt sich das Eisen nämlich ziemlich schnell in Lösung
bringen und zwar in Stücken, wie sie bei der Elektrolyse angewandt werden können,
ohne daß Wasserstoff oder Kohlensäure sich entwickelt, und zwar wird dieß erreicht,
wenn man dem Wasserstoff, wie er durch die Einwirkung der Säure auf das Eisen frei
wird, einen leicht zu reducirenden Körper wie Chromsäure bietet, und somit dem
Kohlenstoff gegenüber, ihn unwirksam macht.
Eine in der Kälte gesättigte Lösung von doppelt-chromsaurem Kali mit dem
gleichen Volum Wasser verdünnt und mit so viel Schwefelsäure versetzt als zur
Sättigung des Kalis des resultirenden Chromoxydes und Eisenoxydes erforderlich ist,
besitzt die Eigenschaft, Eisen, welches in sie eingesenkt ist, ohne Gasentwickelung
zu lösen. Befindet sich dasselbe wie bei der Elektrolyse dicht unter der Oberfläche,
so bleibt der Kohlenstoff unafficirt zurück, während das Eisen als concentrirte
Oxydlösung in Schlieren nach dem Boden des Gefäßes herabsinkt; es geht in Folge
dessen die Farbe der Lösung sehr bald in eine undurchsichtig braune über. Die Lösung
erfolgt hier ebenso rasch wie durch Elektrolyse, doch bleibt bei diesem Proceß eine
außerordentlich eisenhaltige Kohle zurück, die offenbar als eine chemische
Verbindung beider anzusehen ist; sie ist sehr weich, stark abfärbend mit
metallischem Glanze, wie feingepulverter Graphit, löst sich, wenn Stahl angewandt
worden, in Salzsäure unter lebhafter Wasserstoff- und
Kohlenwasserstoff-Entwickelung klar auf. Es ist dieses Verfahren
vorzuschlagen vorzüglich für Stahl und weiches Eisen, während bei Anwendung von
Spiegeleisen stets eine wenn auch schwache Wasserstoff- und
Kohlenwasserstoff-Entwickelung beobachtet wurde; vielleicht jedoch, daß bei
Anwendung concentrirterer Chromsäure-Lösungen auch hier dieser Mißstand sich
heben ließe.
Tafeln