| Titel: | Bestimmung des Ammoniaks im Gaswasser. |
| Fundstelle: | Band 236, Jahrgang 1880, S. 486 |
| Download: | XML |
Bestimmung des Ammoniaks im
Gaswasser.
Mit einer Abbildung auf Tafel 42.
Foster's Bestimmung des Ammoniaks im Gaswasser.
Bei der Bestimmung des Ammoniakgehaltes von Gaswasser durch directes Titriren wird
meist zu wenig gefunden, da nur das freie und an Kohlensäure gebundene Ammoniak
gemessen wird, während bei der vorherigen Destillation mit Kali durch theilweise
Zersetzung von Cyan oft zu viel gefunden wird. W.
Foster empfiehlt nun im Journal für
Gasbeleuchtung, 1880 S. 45 zu der Bestimmung als Stickstoff mittels
unterbromigsaurem Natron nach der Formel: 2NH3 +
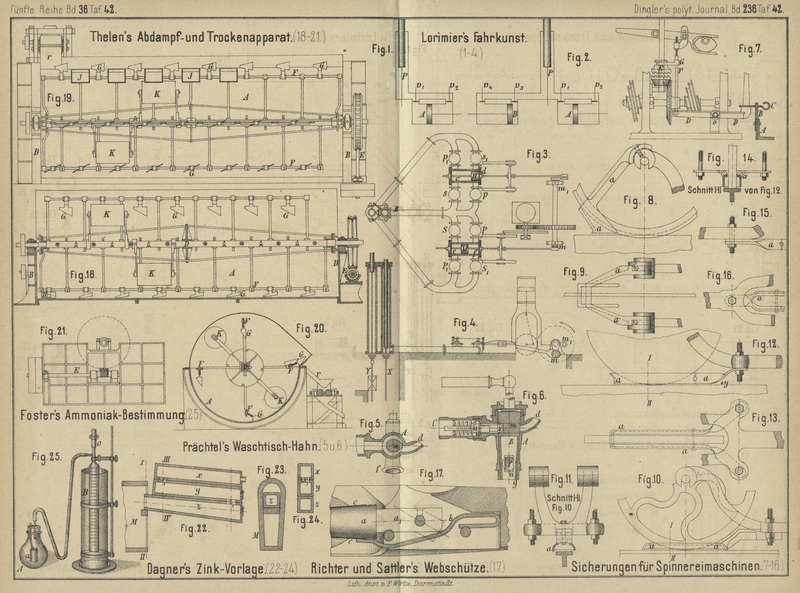
3NaOBr = N2 + 3NaBr + 3H2O den in Fig. 25
Taf. 42 dargestellten Apparat.
Zunächst löst man 4g Natron in Wasser zu 10cc auf, fügt 1g
Brom hinzu, schüttelt um und bringt diese Flüssigkeit in die Flasche A. Das an einem Glasstabe hängende kleine Glasgefäſs
a nimmt das zu untersuchende Gaswasser auf. Man
taucht nun den Meſscylinder B so weit in das Wasser des
gröſseren Cylinders, daſs die Flüssigkeit innen und auſsen auf Null steht, und
schlieſst dann den aufgesetzten Gummischlauch o mittels
Quetschhahn oder eingeschobenen Glasstab ab. Durch Auf- und Abheben der Glocke kann
man sich überzeugen, ob der Apparat vollständig dicht schlieſst; ist dies der Fall,
so schüttelt man das Glaskölbchen um, so daſs allmählich das Ammoniakwasser aus dem
aufgehängten Gefäſs herausflieſst und mit der bromirten Lauge zusammenkommt. Da die
Reaction von einem lebhaften Schäumen begleitet ist, so erfordert dieselbe einige
Vorsicht. Nachdem die beiden Flüssigkeiten vollständig gemischt sind und die
Gasentwicklung beendet ist, kann man das Kölbchen erwärmen, um allen noch gelösten
Stickstoff auszutreiben. Man läſst alsdann wieder auf die ursprüngliche Temperatur
abkühlen, liest an dem Meſscylinder das Volumen des entwickelten Stickstoffes ab und
berechnet daraus in bekannter Weise den Ammoniakgehalt unter Berücksichtigung, daſs
mit diesem Verfahren 4 Proc. zu wenig gefunden werden.
Tafeln