| Titel: | H. N. Morse und A. F. Linn's Bestimmung der Salpetersäure. |
| Fundstelle: | Band 262, Jahrgang 1886, S. 370 |
| Download: | XML |
H. N. Morse und A. F. Linn's Bestimmung der
Salpetersäure.
Mit Abbildung auf Tafel
24.
Morse und Linn's Bestimmung der Salpetersäure.
Die von H. N. Morse und A. F.
Linn (Scientific American Supplement, 1886 * S. 8964 nach dem American Chemical Journal) vorgeschlagene Methode zur
Bestimmung der Salpetersäure ist eine Abänderung des Verfahrens von Tiemann-Schulze. Die Salpetersäure wird ähnlich wie
beim letzteren Verfahren mit Eisenchlorür und concentrirter Salzsäure zu Stickstoffoxyd NO reducirt und letzteres durch Kochen
ausgetrieben, dann aber nicht gasförmig aufgefangen, sondern in eine titrirte Lösung
von Kaliumpermanganat geleitet. Die Oxydation verläuft
nach folgender Gleichung: 6KMnO4 + 10NO = 3K2O + 6MnO + 5N2O5. Um eine leichtere Absorption des Stickstoffoxydes zu bewirken,
empfehlen Morse und Linn,
der Permanganatlösung etwas schwefelsaures Zink zuzusetzen. Zur Verhinderung einer
Oxydation des NO zu NO2 muſs vor Beginn der
Zersetzung die Luft vollständig aus dem Apparate entfernt werden, was durch Füllen
des ganzen Apparates mit Kohlensäure erreicht werden soll.
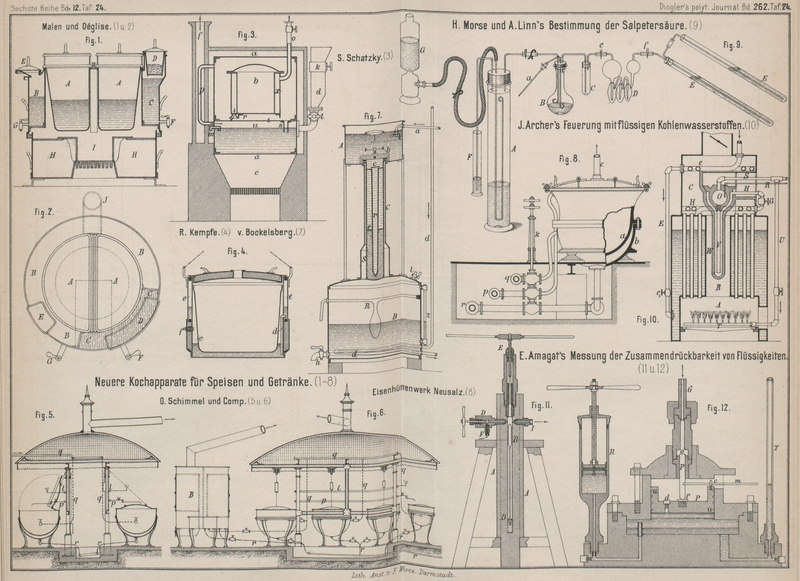
Morse und Linn bedienen sich dazu der in Fig. 9 Taf. 24
dargestellten Vorrichtung. In dem Cylinder A befindet
sich eine gesättigte Lösung von doppeltkohlensaurem Natron mit überschüssigem festem
Salz, während das höher stehende Gefäſs G mit der zur
Zersetzung des Natriumbicarbonates dienenden verdünnten Schwefelsäure gefüllt ist,
deren Zufluſs durch einen Quetschhahn geregelt werden kann. Um das Gas unter höherem
Drucke zu halten, führt aus A ein Rohr in den Cylinder
F, welcher theilweise mit Quecksilber gefüllt ist.
Die Anwendung von Marmor zur Kohlensäure-Entwickelung wird von Morse und Linn verworfen,
weil nach ihren Versuchen selbst nach 20stündigem Einliegen in kochendem Wasser
nicht alle Luft aus dem Marmor verdrängt war. Der Kolben B, dessen Einrichtung aus Fig. 9 ersichtlich ist,
erhält die zu prüfende Substanz. Das Kölbchen C dient
zur Verdichtung der überdestillirten Salzsäure, während die letzten Spuren derselben
in dem mit einer Lösung von kohlensaurem Kali gefüllten Geißler'schen Apparate D zurückgehalten
werden. Die Permanganatlösung befindet sich in den Röhren E.
Bei Beginn des Versuches wird der Apparat vollkommen mit
Kohlensäure gefüllt und darauf die in B befindliche
neutrale oder alkalische Flüssigkeit zum Sieden erhitzt. Nach einiger Zeit schlieſst
man die Hähne e und f,
läſst B abkühlen und saugt dann durch das Rohr a Eisenchlorürlösung und Salzsäure in den Kolben.
Darauf wird das Erhitzen zur Zersetzung der Salpetersäure und zum Austreiben des
gebildeten Stickstoffoxydes wieder aufgenommen, wenn nothwendig auch unter
nochmaligem Einsaugen von Eisenchlorür und Salzsäure. Die letzten Spuren von NO
werden schlieſslich durch einen langsamen Strom von Kohlensäure aus dem Apparate
verdrängt.
Um die zur Oxydation verbrauchte Menge Permanganat zu ermitteln,
versetzen Morse und Linn
die Flüssigkeit aus der Röhre E mit überschüssiger
Oxalsäurelösung von bekanntem Gehalte und titriren den Ueberschuſs an letzterer mit
Permanganatlösung zurück. Die erhaltenen Zahlen sind sehr befriedigend. Es wurden
bei 9 Versuchen je 100 bis 200mg Kaliumnitrat
verwendet; die gröſste Abweichung zwischen dem gefundenen und dem berechneten Werthe
betrug 0cc,05. Bei dem Versuche, die
Oxalsäurelösung durch eine Lösung von schwefelsaurem Manganoxydul von bekanntem
Gehalte zu ersetzen, wurden ebenfalls noch befriedigende Zahlen erhalten; doch wurde
die mit Oxalsäure erzielte Genauigkeit nicht erreicht.
Tafeln