| Titel: | Neue Verfahren und Apparate der Soda-Industrie. |
| Autor: | Sachse |
| Fundstelle: | Band 267, Jahrgang 1888, S. 356 |
| Download: | XML |
Neue Verfahren und Apparate der
Soda-Industrie.
Patentklasse 75. Mit Abbildungen im Texte und auf
Tafel 17.
Neue Verfahren und Apparate der Soda-Industrie.
Um aus Rohsoda des Leblancprozesses, aus rohem
Schwefelnatrium oder aus rohem Bicarbonat des Ammoniaksodaprozesses nahezu chemisch
reines Bicarbonat zu gewinnen, lösen N. Mathieson und
J. Hawliczek in Liverpool (D. R. P. Nr. 41985 vom
7. Januar 1887) die betreffenden Rohproducte in 16 bis 19procentiger Salzsoole auf
und behandeln die Lösung mit Kohlensäure, wodurch nahezu alles Natron der Rohstoffe
als reines Bicarbonat in krystallinischer Form ausgeschieden wird, welches durch ein
Vacuumfilter oder eine Centrifuge von der Salzsoole getrennt wird. Mit kleiner, aber
hinreichender Menge Wasser systematisch gewaschen, resultirt ein Bicarbonat von
nahezu chemisch reiner Form. Bei rationeller Leitung des Prozesses wird man nur so
viel Waschwasser zu verwenden suchen, als Wasser aus der Rohlauge durch Bildung des
Natriumbicarbonates in fester Form entnommen ist und dadurch eine constante Soole
von 16 bis 19 Proc. Kochsalz zur Auflösung neuer Mengen von Rohsoda im Kreislauf des
Prozesses erhalten. Bei der Verarbeitung von Rohsoda und rohem Schwefelnatrium ist
es nöthig, durch Einleiten von Kohlensäure zunächst Kieselsäure, Eisen und Thonerde
zu fällen und dieselbe bei beginnender Bicarbonatausscheidung von der Lauge durch
Filtration zu trennen und dann erst die Abscheidung des Bicarbonates durch weiteres
Einleiten von Kohlensäure zu bewirken. Diese Abscheidung der genannten
Verunreinigung findet bei der Verarbeitung von rohem Bicarbonat bereits durch das
Auflösen desselben in der heiſsen Soole statt, wobei das Bicarbonat zum groſsen
Theile unter Abgabe von Kohlensäure in Monocarbonat übergeführt wird. Die hierbei
entweichende Kohlensäure und das dem Rohbicarbonat anhaftende und nun ebenfalls
entweichende Ammoniak werden aufgefangen, ebenso wie der bei der Verarbeitung von
Rohschwefelnatrium ausgetriebene Schwefelwasserstoff. In gleicher Weise wie
Chlornatrium soll auch Natriumsulfat in Form von Laugen bei dem beschriebenen
Verfahren verwendet werden.
Bei dem Ammoniaksodaverfahren gibt die bei der Ausscheidung des Bicarbonates aus der
ammoniakalischen Kochsalzlauge frei werdende Wärme leicht zu einer allzu starken
Erhitzung des Apparates Veranlassung, so daſs schlieſslich wieder eine Zersetzung
des Bicarbonates eintreten kann, was bekanntlich bei etwa 60° der Fall ist. Tritt
eine derart hohe Hitze auch nicht ganz ein, so wirkt doch schon eine annähernde
Erwärmung höchst nachtheilig auf die Ausscheidung des Bicarbonates. Durch Anbringung
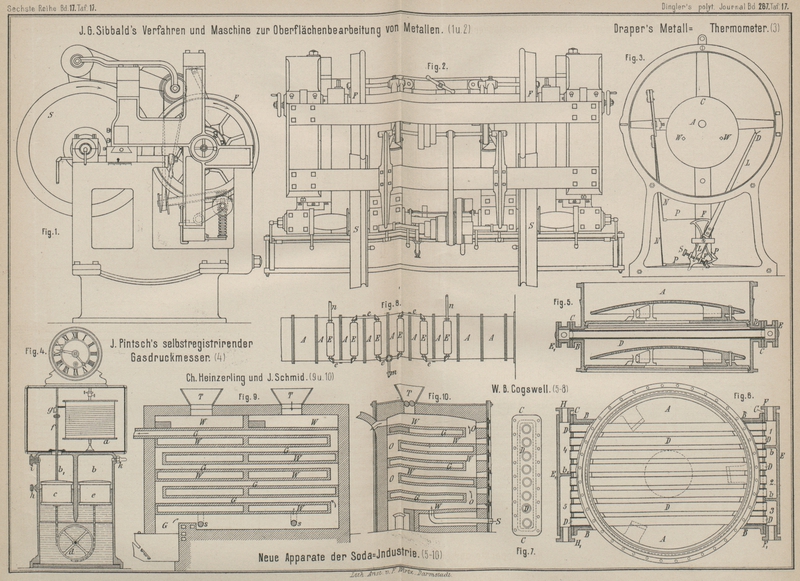
einer Kühlvorrichtung an der gewöhnlichen Reactionscolonne sucht W. B. Cogswell in Syracuse (* D. R. P. Nr. 41989 vom 8.
Februar 1887) diesen Uebelstand zu vermeiden. Zu dem Ende sind die Colonnenelemente
A (Fig. 5 bis 8 Taf. 17) an zwei
gegenüberliegenden Seiten mit rechteckigen Oeffnungen versehen, welche durch
entsprechende Stutzen B eingeschlossen werden. Die vorn
gerade abgeglichenen Stutzen B sind hier mit einem
gelochten Flansch versehen, auf welchem eine am Rande ebenso gelochte Platte C befestigt wird. Diese Platte C ist im mittleren Theile mit Löchern versehen, in welchen die durch das
Element hindurch reichenden Kühlrohre D in irgend einer
geeigneten Weise abgedichtet werden. Die Rohrenden liegen in Behältern, welche nach
innen zu durch die Platten C, nach auſsen hin durch die
Deckel E bezieh. E1 abgeschlossen werden. Der Deckel E ist mit zwei Stegen b
versehen, welche bis auf die Platte C reichen und den
Deckelraum derart in drei Abtheilungen 1, 2, 3 theilen,
daſs in den Endräumen 1 und 3 sich je zwei und in dem mittleren Raume 2
sich vier Rohrmündungen befinden. Der an den gegenüberliegenden Rohrenden
befindliche Deckel E1
ist nur in der Mitte mit einem Steg b1 versehen, so daſs in jede der hier entstehenden
beiden Abtheilungen 4 und 5 vier Rohre ausmünden.
Das Kühlwasser flieſst durch Rohr m zu und tritt durch
den Anschluſsstutzen F in die Abtheilung 1 ein, flieſst durch die beiden hier einmündenden Rohre
D in die auf der gegenüberliegenden Seite des
Elementes befindliche Abtheilung 4, tritt in die beiden
benachbarten Rohre D über und gelangt nach der
Abtheilung 2, aus welcher es durch die beiden nächsten
Rohre nach der Abtheilung 5 flieſst, um durch die
beiden letzten Rohre schlieſslich nach der Abtheilung 3
zu kommen. Aus dieser flieſst es durch den Stutzen F1 und das Verbindungsrohr e (Fig.
8) nach der Kühlvorrichtung des nächsten Elementes über. Nachdem das
Kühlwasser mehrere Elemente passirt hat, flieſst es durch eines der Rohre n ab. An den Abtheilungen 4 und 5 sind ebenfalls Rohrstutzen H bezieh. H1 angebracht, welche ebenfalls zur Verbindung der
Kühlvorrichtung der einzelnen Elemente dienen können. Die Elemente selbst werden in
der bei solchen Colonnen üblichen Weise auf einander befestigt.
Von Solvay selbst ist bereits die Magnesia zur
Zersetzung der beim Ammoniaksodaprozeſs abfallenden Salmiaklauge, sowie die
Gewinnung von Salzsäure aus dem hierbei resultirenden Chlormagnesium durch Erhitzen
desselben mit
Kieselsäure oder Thonerde vorgeschlagen. Diese oder auch anderweitige Zerlegung des
Chlormagnesiums hat bisher noch nicht vortheilhaft in der Praxis durchgeführt werden
können, und es ist dies einer der wenigen wunden Punkte des Ammoniaksodaprozesses,
welcher bisher das Gesammtchlor des Kochsalzes in Form von unverwerthbarem
Chlorcalcium oder Chlormagnesium verliert. Dr. Chr.
Heinzerling und Dr. J. Schmid in Zürich (* D.
R. P. Nr. 41996 vom 24. März 1887) wollen die völlige Zerlegung des
Magnesiumchlorides unter Gewinnung eines Stromes concentrirten Salzsäuregases
dadurch bewirken, daſs sie das beim Entwässern und bei der hierbei statthabenden
theilweisen Zersetzung des Magnesiumchlorides sich ergebende Gemenge von Wasserdampf
und Salzsäuregas über das bereits entwässerte und in Muffeln erhitzte Magnesiumchlorid bezieh. Magnesiumoxychlorid systematisch
leiten, so daſs das heiſse Gemenge von Dampf und Salzsäuregas zunächst über schon
ziemlich vollständig in Magnesia übergeführtes Magnesiumchlorid und das sich an
Salzsäure fortwährend bereichernde Dampfgemenge schlieſslich über frisches, nur
entwässertes Magnesiumchlorid bezieh. Oxychlorid geführt wird, so daſs zum Schluſs
ein durch Rauchgase nicht verunreinigtes concentrirtes Salzsäuregas den
Zersetzungsofen verläſst. Dieser Ofen (Fig. 9 und 10 Taf. 17) ist ein
Etagenmuffelofen, dessen einzelne Etagen durch die durch G von unten heraufströmenden und verbrennenden Generatorgase zum Glühen
erhitzt werden, so daſs die untersten Etagen naturgemäſs die stärkste Glut besitzen.
Das bei der ersten Entwässerung bezieh. theilweisen Zersetzung des
Magnesiumchlorides resultirende Magnesiumoxychlorid wird noch heiſs durch die mit
Speisewalzen versehenen Trichter T auf der obersten
Etage ausgebreitet und nach bestimmten Zeitintervallen mit Krücken von einer Etage
durch die bald hinten, bald vorn liegenden Unterbrechungen O auf die nächst darunter liegende Etage geschafft. Die bei der ersten
Zersetzung des Magnesiumchlorides entweichenden Producte, bestehend aus Salzsäuregas
und Wasserdampf, streichen nun durch JFin umgekehrter Richtung, nachdem sie in der
Röhre s überhitzt worden sind, von unten nach oben über
das glühende Magnesiumoxychlorid weg, wodurch dasselbe successive in Magnesia und
Chlorwasserstoffsäure zerlegt wird, welch letztere nun ihrerseits die anfangs
verdünnte Salzsäure systematisch anreichert. Durch dieses eigenthümliche
Gegenstromprinzip wird es ermöglicht, mit wenig mehr als dem im sechsfach
gewässerten Chlormagnesium enthaltenen Wasser alle Salzsäure auszutreiben, das
Chlormagnesium zu spalten in Magnesia und eine concentrirte Salzsäure. Da das
Salzsäuregas weder durch die Rauchgase noch durch erhebliche Mengen von Luft
verdünnt ist (letztere dringt nur ein beim jeweiligen Oeffnen der Arbeitsthüren), so
dürfte die Codensation der Salzsäure keine besonderen Schwierigkeiten bieten, welche
wohl mehr der Etagenofen selbst durch Undichtheiten u.s.w. bereiten dürfte.
Nach Versuchen von Dr. Löwig in Breslau (D. R. P. Nr.
41990 vom 9. Februar 1887, abhängig vom Patent Nr.
21593) hat sich das durch Erhitzen von Natriumbicarbonat des Ammoniaksodaprozesses
erhaltene kohlensaure Natron als besonders geeignet erwiesen, nach dem durch Patent
Nr. 21593 geschützten Verfahren durch Erhitzen mit Eisenoxyd in Aetznatron übergeführt zu werden. Hierbei kann das rohe Natriumbicarbonat des Ammoniakprozesses direkt mit
der nöthigen Menge Eisenoxyd gemischt und dann diese Mischung behufs Darstellung des
Aetznatrons geglüht werden, und empfiehlt es sich, das Glühen der letztgenannten
Mischung zunächst in einem geschlossenen Apparate vorzunehmen, wie man solche
gegenwärtig in den Ammoniaksodafabriken zur Umbildung des Natriumbicarbonates in das
Natriummonocarbonat verwendet, welcher Apparat das Auffangen und die
Wiederverwendung des sich bei der Operation entwickelnden Ammoniaks und der
Kohlensäure gestattet.
Hierauf bringt man das noch warme, in diesem geschlossenen Apparate dargestellte
Gemisch von Natriummonocarbonat und Eisenoxyd in einen zweiten Apparat oder Ofen, in
welchem man es behufs Austreibung der noch vorhandenen Kohlensäure der gewünschten
Glühhitze aussetzt, um Aetznatron darzustellen.
Textabbildung Bd. 267, S. 359 In der Praxis hat sich herausgestellt, daſs sich die Alkali- und
Eisenoxydmischung kurz nach eingetretener Reaction mit einer Atmosphäre fast reiner
Kohlensäure umgibt, welche aus der Reaction selbst herrührt. In einer solchen
Atmosphäre schreitet die Reaction nur sehr langsam vorwärts. Auch im gewöhnlichen
Flammofen verbleibt die Kohlensäure, welche viel schwerer als die den Glühraum
durchstreichenden heiſsen Gase ist, in der Nähe der Ofensohle, hüllt die verwendeten
Körper ein und verhindert so eine genügend schnelle und vollständige Reaction. Es
ist daher nöthig, das zu zersetzende Gemisch möglichst schnell und vollständig auſser Berührung mit
diesen heiſsen Reactionsgasen zu bringen, und hat sich zu diesem Zweck die
Verwendung des in vorstehender Figur dargestellten cylindrischen Röstofens als
praktisch erwiesen. Derselbe dreht sich um seine fast horizontale Achse und ist mit
Chamottesteinen dergestalt ausgekleidet, daſs eine Anzahl radial gerichteter, zur
Cylinderachse parallel laufender Vorsprünge d, d1, d2, d3 entstehen, welche das Reactionsgemisch bei der
Rotation des Ofens auf eine gewisse Höhe heben und dann durch die den Ofen
durchziehenden heiſsen Feuergase herabfallen lassen, wobei die innerhalb der Masse
gebildete fast reine Kohlensäure durch die heiſsen Feuergase ersetzt wird und mithin
den Verlauf und Vollzug der Reaction der Alkali- und Eisenoxydmischung nicht
beeinträchtigen kann. Zur Erläuterung der dargestellten Anlage diene noch
Folgendes:
a ist der mit feuerfesten Steinen ausgelegte Cylinder,
welcher von einem geeigneten Riemenantriebe aus durch die Zahnräder b, b1 in Drehung
versetzt wird, von denen b1 auf der Ofenauſsenfläche sitzt; geeignete Tragscheiben c, c1, auf denen zwei
auf der Cylinderauſsenfläche aufgeschobene, befestigte Ringe laufen, sichern den
Cylinder und schützen ihn gegen Durchbiegen, e ist der
Feuerherd zur Bildung der heiſsen Verbrennungsproducte, f der Abzugskanal, g ein Aufgebetrichter.
Lagerung findet der Cylinder bei seiner Drehung einerseits auf dem Abzugskanal des
Herdes, andererseits auf einem an den Abzugskanal sich anschlieſsenden Ansätze.Vgl. Die Metallurgie von Percy-Wedding 2. Bd. * S. 300 Danks
Ofen. Arents 1887 264 * 617. Smith 1888 267 * 37.
F. P. E. de Lalande in Paris (D. R. P. Nr. 41991 vom 22.
Februar 1887) macht das durch Entschwefelung von Alkali- und Erdalkalisulfiden
bisher vorgeschlagene Zinkoxyd behufs Darstellung von
Aetzalkalien und Hydraten der alkalischen Erden durch Behandlung mit Aetzalkalien besonders reactionsfähig, da nach seinen Erfahrungen nur das
durch Verbrennung von Zink erhaltene Zinkoxyd ohne Weiteres zur Entschwefelung
geeignet ist, während durch Rösten von Zinkblende oder gefälltem Schwefelzink oder
durch Glühen von Galmei hergestelltes Zinkoxyd nur äuſserst langsam und unvollkommen
auf die Alkali- und Erdalkalisulfide einwirken soll. Für diesen Zweck genügt es, das
fein gepulverte Zinkoxyd mit Aetzalkalien zu behandeln, was in der Kälte, Wärme oder
unter Feuerschmelzung bei verschiedener Einwirkungsdauer geschehen kann. In
rationeller Weise wird das Verfahren zur Darstellung von Aetznatron etwa wie folgt ausgeführt:
Man löst 100 Th. festes Aetznatron in 150 Th. Wasser, so daſs man eine Lauge mit etwa
40 Proc. Natron erhält. Dieselbe kocht man etwa ¾ bis 1 Stunde unter sorgfältigem
Umrühren und unter Zugabe von ungefähr 100 Th. Zinkoxyd, z.B. von geglühtem Galmei,
gerösteter Blende oder regenerirtem, bei dem vorliegenden Verfahren gewonnenem Zinkoxyd. Nun fügt man
unter fortgesetztem Kochen und Umrühren eine warme, concentrirte
Schwefelnatriumlösung mit 38 bis 40 Proc. Schwefelnatrium (Na2S), welches eine sofortige Umsetzung erfährt, so
lange zu, bis sich ein ganz geringer Ueberschuſs an Schwefelnatrium zeigt, was man
daran erkennen kann, daſs ein Tropfen der klaren Flüssigkeit eine Lösung von
Nickelammoniumsulfat dunkel färbt.
Zu dem ganzen Gemenge, welches auſser den anfangs gebrauchten 100 Th. noch das so
gebildete Aetznatron, z.B. 50 Th., enthält, fügt man eine diesem gesammten
Aetznatron entsprechende Menge Zinkoxyd, für vorliegenden Fall z.B. 150 Th., und
kocht wiederum ¾ bis 1 Stunde, worauf man in vorhin beschriebener Weise
Schwefelnatrium zugibt, dessen Menge jetzt selbstverständlich eine entsprechend
gröſsere ist.
Sobald der Kessel genügend gefüllt ist, läſst man, die Hälfte der Masse heraus und
benutzt den zurückbleibenden Theil zur weiteren Operation, indem man wieder eine
entsprechende Menge Zinkoxyd hinzugibt, um dasselbe durch Kochen mit der
Aetznatronlauge reactionsfähig zu machen und dadurch eine neue Menge von
Schwefelnatrium in Aetznatron umzusetzen.
Jede Operation, zu welcher man die Herstellung des reactionsfähigeren Zustandes des
Zinkoxydes und das Verwandeln des Schwefelnatriums in Aetznatron durch dieses
reactionsfähige Zinkoxyd zu rechnen hat, dauert 1½ bis 2 Stunden. Die Reaction
selbst verläuft fast genau der Theorie entsprechend.
Das in Lösung befindliche Aetznatron trennt man von dem Schwefelzink auf geeignete
Weise, z.B. durch Filterpressen, wodurch man eine concentrirte Lauge gewinnt, aus
welcher reines, festes Aetznatron durch Abdampfen und, wenn nöthig, durch Reinigung
nach einem bekannten Verfahren gewonnen werden kann. Das Schwefelzink wird
getrocknet, in geeigneter Weise geröstet und als Zinkoxyd, nachdem es in oben
beschriebener Weise reaktionsfähig gemacht worden ist, für die Fabrikation zur
Aetzendmachung von Schwefelalkali verwendet.
Behufs Darstellung der Hydrate der alkalischen Erden setzt man zu der aus Zinkoxyd
und Natron bestehenden Masse so viel Schwefelbarium oder Schwefelstrontium, als von
diesen Sulfiden zersetzt werden kann. Darauf entfernt man das entstandene
Schwefelzink durch Decantation, Filtration und Waschen; das Schwefelzink wird zur
Herstellung von Zinkoxyd benutzt; aus der Lösung gewinnt man durch Krystallisation
die alkalischen Erden.
Die Mutterlauge, welche neben etwas Aetzbaryt bezieh. Aetzstrontian zum gröſsten
Theile Aetznatron enthält, kann zur Behandlung des z.B. aus dem Schwefelzink
gewonnenen Zinkoxydes benutzt werden. Will man den Aetzbaryt oder das Aetzstrontian
aus dieser Mutterlauge entfernen, was nicht immer nöthig ist, so kann man das leicht
durch Zusatz von Natriumsulfat erreichen.
Man kann auch das mit Natronlauge behandelte Zinkoxyd von der Lauge durch Filtration
oder Decantation trennen und durch Auswaschen reinigen., dieses gereinigte Zinkoxyd
der Behandlung mit Baryum- oder Strontiumsulfid unterwerfen, wodurch sogleich reiner
Aetzbaryt oder reines Aetzstrontian neben Zinksulfid entstehen. Die von dem Zinkoxyd
getrennte Natronlauge kann wieder dazu verwendet werden, Zinkoxyd reactionsfähig zu
machen.
Um aus unreinem festen Natriumchlorid, wie solches in
der Natur als unreines Steinsalz und ebenso als industrieller Abfall vorkommt, reines Natriumchlorid zu gewinnen, schlägt Dr. P. Degener in Berlin vor, den unreinen Rohstoff aus
einer heiſsen Chlorcalciumlauge von etwa 1,1 spec. Gew. umzukrystallisiren, welche
beim Erkalten Natriumchlorid in fast chemisch reiner Form fallen läſst. (D. R. P.
Nr. 42422 vom 10. April 1887.)
Die zurückbleibende Mutterlauge, welche neben dem Natriumchlorid auch die in ihr
löslichen Nebenbestandtheile des Rohsalzes enthält (das sind vornehmlich Magnesium-
und Calciumchlorid) wird im Wesentlichen auf ihre ursprüngliche Zusammensetzung
dadurch wieder zurückgeführt, daſs man sie zeitweilig oder continuirlich mit
gebranntem oder gelöschtem Kalk behandelt; auch gebrannter oder gelöschter Dolomit
ist anwendbar. Dabei entsteht aus dem Magnesiumchlorid Calciumchlorid, welches neben
dem im Rohsalz an und für sich enthaltenen der Anreicherung der Lösung zu gute
kommt. Nebenher wird Magnesiahydrat ausgeschieden.
Das Magnesiumsulfat des Rohsalzes wird schon bei der Auslaugung in Calciumsulfat und
Magnesiumchlorid umgesetzt. Aus Natriumsulfat entsteht ebenfalls Calciumsulfat und
Natriumchlorid. Sollten die beiden genannten Sulfate daher im Rohsalz sich finden,
so geben sie nur zur Entstehung von Magnesium- und Natriumchlorid Veranlassung;
Calciumsulfat ist in concentrirten Calciumchloridlaugen so gut wie unlöslich.
Auf diese Weise wird die Raffination des Rohsteinsalzes u.s.w. durch einen einfachen
Umkrystallisationsprozeſs ohne jede bedeutendere Verdampfung erzielt.
Sachse.
Tafeln