| Titel: | Ueber das Platin und die es begleitenden Metalle; von H. Sainte-Claire Deville und H. Debray. |
| Fundstelle: | Band 154, Jahrgang 1859, Nr. LXXXII., S. 384 |
| Download: | XML |
LXXXII.
Ueber das Platin und die es begleitenden Metalle;
von H. Sainte-Claire
Deville und H.
Debray.
(Schluß von S. 295 des vorhergehenden
Heftes.)
Mit Abbildungen auf Tab.
II.
Deville, über das Platin und die es begleitenden
Metalle.
VII. Darstellung des Osmiums,
Rutheniums, Rhodiums und Iridiums in reinem Zustande.
1. Osmium.
Um das Osmium in cohärentem Zustande, von einer Dichtigkeit gleich derjenigen des
Platins (21,4) zu erhalten, verfährt man folgendermaßen. Man nimmt
pulverförmiges Osmium-Iridium, welches durch ein Seidensieb passirt
wurde. (Wenn dasselbe nicht ursprünglich pulverförmig ist, kann man es mittelst
des unten für das Ruthenium angegebenen Verfahrens chemisch zertheilen.) 1 Thl. solchen
Osmium-Iridiums vermengt man mit 5 1/2 Theilen Baryumsuperoxyd, welches
man mit der größten Sorgfalt abwiegt, um es später durch ein bekanntes Gewicht
Schwefelsäure gänzlich fällen zu können. Dieses Gemenge, welches durch
andauerndes Zereiben in einem Porzellanmörser so innig als möglich gemacht
worden seyn muß, erhitzt man in einem hessischen Tiegel, auf welchem sein Deckel
angebracht und mit ein wenig Lehm lutirt worden ist, 1–2 Stunden lang auf
den Schmelzpunkt des Silbers. Nach dem Erkalten findet man im Tiegel eine
schwarze, homogene Masse, welche man gröblich zertheilt und in eine Glasretorte
gibt. Man gießt in dieselbe zuerst ein wenig Wasser, dann 8 Theile Salzsäure und
1 Theil gewöhnlicher Salpetersäure, rührt um und destillirt, wobei man die
Vorlage der Retorte mit der größten Sorgfalt abkühlen muß, damit nicht
Osmiumsäure-Dämpfe verloren gehen. Die Operation ist beendigt, wenn durch
den Tubulus der Retorte ausgelassener Dampf nicht mehr den charakteristischen
Geruch der Osmiumsäure besitzt. Die in der Vorlage enthaltene Flüssigkeit wird
wieder destillirt, wobei man in den vorgeschlagenen tubulirten Ballon verdünntes
Ammoniak bringt. Das so erhaltene osmiumsaure Ammoniak übersättigt man mit
Schwefelwasserstoff, erhält die das Schwefelosmium enthaltende Flüssigkeit lange
Zeit im Sieden, und filtrirt dann. – Man darf das Filter nicht bei einer
zu hohen Temperatur trocknen, weil sonst das Schwefelosmium sich entzündet, wobei es sich in Osmiumsäure und
schweflige Säure verwandelt. Das Schwefelmetall gibt man in einen Tiegel aus
Gaskohks, welcher innerlich ganz glatt und mit einem dicht aufpassenden Deckel
versehen ist; derselbe wird in einen Tiegel aus feuerfestem Thon gestellt, der
Zwischenraum beider Tiegel mit Sand gefüllt, der thönerne Tiegel mit einem guten
Deckel geschlossen und die Hitze dann vier bis fünf Stunden lang auf dem
Schmelzpunkt des Nickels erhalten.Im Loboratorium der Normalschule zu Paris benutzt man als Brennmaterial,
um diese hohe Temperatur zu erzielen, Abfälle von Gaskohks, welche zu
hart sind, um daraus Elemente für die Bunsen'sche Säule schneiden zu können. Diese Gaskohks, welche
keine Asche hinterlassen, greifen die Tiegel nicht an; die nicht
hinreichend feuerbeständigen Tiegel werden durch sie zwar erweicht, aber
deren Wände nicht zerstört, wie durch die Schlacke der gewöhnlichen
Kohks. Die Gaskohks sind zwar schwierig zu entzünden, brennen aber
außerordentlich kräftig.
Das Schwefelosmium ist durch die Hitze reducirbar und hinterläßt ein glänzendes
Metall, welches eine hellere bläuliche Farbe als das Zink hat, in kleinen
Stücken, die sich sehr leicht zertheilen. Dieses Osmium hat keinen Geruch; man
kann es auf den Schmelzpunkt des Zinks erhitzen, ohne daß sich
Osmiumsäure-Dämpfe bilden; bei einer höheren Temperatur wird es aber
brennbar.
Um das Osmium krystallisirt zu erhalten, erhitzt man
es in einem Kohlentiegel mit seinem 7 bis 8fachen Gewicht Zinn auf die lebhafte
Rothglühhitze, bis es darin aufgelöst ist, und läßt dann die Metallmasse langsam
abkühlen; im Moment des Erstarrens scheidet sich das Osmium vom Zinn ab, indem
es krystallisirt. Man braucht dann bloß das Zinn in Salzsäure aufzulösen, um ein
sehr hartes krystallinisches Pulver zu erhalten, welches kein Zinn zurückhält,
ohne daß die Säure merklich Osmium auflöst.
2. Ruthenium.
Das Ruthenium ist das feuerbeständigste unter den Metallen des Platinerzes. Man
kann es nur schmelzen, wenn man es in 1–2 Millimeter Entfernung vom Ende
des Knallgas-Löthrohrs anbringt, an dem Punkt wo die höchste Temperatur stattfindet; dabei verflüchtigt sich
Rutheniumoxyd, welches einen ähnlichen Geruch wie die Osmiumsäure hat und einen
braunen Anflug bildet. Das Ruthenium ist spröde und hart wie das Iridium; reines
geschmolzenes Ruthenium hat eine Dichtigkeit von 11 bis 11,4.
Um das Ruthenium darzustellen, legirt man rutheniumhaltiges Osmium-Iridium
in Blättern mit seinem vier- bis fünffachen Gewicht Zink und verjagt dann
letzteres durch Hitze; hierzu gibt man die gemengten Materialien in einen
geeignet geschützten Kohlentiegel, worin man sie zuerst eine Stunde lang auf der
bloßen Rothglühhitze erhält, dann zwei Stunden lang auf der Weißglühhitze, bis
aus der Flamme aller Zinkdampf verschwunden ist. Man findet im erkalteten Tiegel
eine zerreibliche poröse Masse, welche genau so viel wiegt wie das angewandte
Osmium-Iridium. Diese Masse läßt sich leicht zerpulvern, bis auf ein
kleines Quantum von Schuppen, welche man durch das Seidensieb absondert. Man
vermengt höchst sorgfältig 1 Theil des feinen Pulvers mit 3 Thl. Baryumsuperoxyd
und 1 Thl. salpetersaurem Baryt, und bringt das Gemenge in einen hessischen
Tiegel, welchen man zum Rothglühen (auf eine Temperatur etwas unter dem
Schmelzpunkt des Silbers) eine Stunde lang erhitzt. Nach dem Erkalten findet man
darin eine schwarze, zerreibliche Masse, welche man höchst sorgfältig
pulverisirt und dann in eine Flasche mit eingeschliffenem Stöpsel schüttet, in
die man vorher 20 Thle. Wasser und 10 Thle. gewöhnliche Salzsäure gegeben hat.
Die Flasche wird in kühles Wasser getaucht, damit sich die Temperatur in Folge
der eintretenden Reaction nicht erhöht. Man schüttet dann den durch die Schmelzoperation
erhaltenen osmium-iridiumsauren Baryt in kleinen Portionen hinein; diese
Operation muß man unter einem gut ziehenden Kamin vornehmen, weil das Chlor oder
der Sauerstoff, welche sich entbinden, ein wenig Osmiumsäure mit sich reißen.
Nachdem die Operation ganz beendigt ist, setzt man 1 Thl. Salpetersäure, dann 2
Thle. gewöhnliche concentrirte Schwefelsäure zu. Man verschließt die Flasche,
schüttelt sie stark und läßt den schwefelsauren Baryt sich absetzen. Man
decantirt, wascht den Niederschlag durch Decantiren aus und destillirt dann alle
vereinigten Flüssigkeiten in einer tubulirten Retorte, bis der vierte Theil
ihres Volums übergegangen ist; das Destillat ist eine an Osmium sehr reiche
Flüssigkeit, welche man sogleich mit Ammoniak und Schwefelammonium fällt. Die in
der Retorte zurückgebliebene rothe Flüssigkeit wird abgedampft, bis sie nur noch
ein kleines Volum einnimmt; man versetzt sie dann mit 2 bis 3 Thln. Salmiak in
Stücken und einigen Kubikcentimetern Salpetersäure; dann dampft man bei einer
Temperatur, welche 100º C. nicht viel überschreiten darf, zur Trockne ab.
Man findet in der Schale einen bläulichschwarzen krystallinischen Niederschlag,
welchen man mit einer kleinen Menge Wasser behandelt, das zur Hälfte mit Salmiak
gesättigt ist, und mit dieser Flüssigkeit auswascht, bis sie sich nicht mehr
färbt. Man bringt das schwarze Salz (chlorwasserstoff- und iridiumsaures
Ammoniak, welches Ruthenium enthält) in einen Porzellantiegel und calcinirt es,
bis die Masse recht roth geworden ist. Es ist zweckmäßig, den Porzellantiegel in
einen hessischen Tiegel zu stellen und in den Zwischenraum beider einige
Kohlenstücke zu legen. Das so erhaltene, mit Ruthenium gemengte Iridium wird in
einem Silbertiegel mit seinem doppelten Gewicht Salpeter und seinem gleichen
Gewicht Kalihydrat 1–1 1/2 Stunden lang bei der Dunkelrothgluth
geschmolzen. Man nimmt die Masse dann in kaltem Wasser auf und filtrirt die
orangegelbe Flüssigkeit, welche rutheniumsaures Kali ist, in einem Trichter
durch Amianth. Diese Flüssigkeit wird mit Kohlensäure oder Salpetersäure
behandelt, bis sich einige Blasen von Kohlensäure, salpetriger Säure oder
Stickoxyd entbinden und die gelbe Farbe ganz verschwunden ist; sie darf gar
nicht nach Osmiumsäure riechen. Sie setzt einen Niederschlag ab, welcher
Rutheniumoxyd, verunreinigt durch ein wenig Kieselerde, ist. Dieses Oxyd
calcinirt man stark in einem Tiegel aus GaskohksWenn das Ruthenium Chromoxyd enthält, so verwandelt sich dieses im Tiegel
in glänzendes und gut krystallisirtes Kohlen-Chrom., und schmilzt es dann mit großer Vorsicht mittelst des früher beschriebenen
kleinen Knallgas-Löthrohrs in einer kleinen Schale, die man in einem
Kalkstück ausgehöhlt hat. Wenn das Ruthenium Osmium, Chrom oder Kieselerde
enthält, so entweichen diese Unreinigkeiten in Dampfform oder verbinden sich mit
dem Kalk.
3. Palladium.
Das Palladium ist von allen Metallen des Platinerzes das leichtflüssigste. In den
zum Schmelzen des Platins dienenden Oefen kommt es mit außerordentlicher
Leichtigkeit in Fluß. Wenn man es mittelst des Knallgas-Löthrohrs der
Schmelzhitze des Iridiums aussetzt, so verschwindet es, wobei es sich dreht und
grüne Dämpfe verbreitet, welche sich zu einem schwarzbraunen Pulver verdichten,
einem Gemenge von Metall und dessen Oxyd. Diesen Versuch muß man auf einer
kleinen Kapelle machen, welche in einem Stück gebrannten Kalks ausgehöhlt ist.
Das Palladium oxydirt sich noch leichter als das Silber bei niederer Temperatur,
daher seine Oberfläche immer durch eine sehr schwache Oxydschicht matt
erscheint.
Die Dichtigkeit des reinen, geschmolzenen und nicht hartgeschlagenen Palladiums
ist 11,4 bei 22º,5 C.
4. Rhodium.
Das Rhodium befindet sich hauptsächlich in den bereits besprochenen Rückständen,
welche man in den Platinfabriken erhält, wenn man die Mutterlaugen von der
Fällung des Platins mittelst metallischen Eisens niederschlägt. Um aus diesen
Rückständen das reine Rhodium darzustellen, schmelzen wir sie vorerst mit ihrem
gleichen Gewicht Blei und ihrem doppelten Gewicht Bleiglätte. Nachdem der Tiegel
gut rothglühend und die Bleiglätte recht flüssig ist, rührt man ein- oder
zweimal um, läßt langsam erkalten, und löst dann den Bleikönig ab, welchen man
gut reinigt; derselbe enthält alle in diesen Rückständen vorkommenden Metalle,
welche weniger oxydirbar als das Blei sind. Man behandelt ihn mit Salpetersäure,
die mit ihrem gleichen Gewicht Wasser verdünnt ist, welche ihm außer dem Blei
auch das Kupfer und Palladium entzieht. Die zurückbleibende pulverförmige und
metallische Substanz wird gut gewaschen, dann äußerst sorgfältig mit ihrem
fünffachen Gewicht pulverisirten Baryumsuperoxyds gemengt, welches man genau
abwiegt. Das Gemenge wird in einem hessischen Tiegel 1–2 Stunden lang der
Rothglühhitze ausgesetzt, dann in Wasser aufgenommen und der verbleibende
Rückstand mit Königswasser behandelt, welches eine große Menge Osmium austreibt,
die man verloren gehen lassen oder durch Destillation als Osmiumsäure sammeln
kann. Nachdem die Flüssigkeit ihren Geruch ganz verloren hat, setzt man ihr so viel
Schwefelsäure zu, daß der Baryt aus dem Gemisch der Chloride ganz abgeschieden
wird. Man läßt kochen und filtrirt; hernach dampft man die Flüssigkeit ab, indem
man ihr zuerst ein wenig Salpetersäure, und dann nach einiger Zeit einen großen
Ueberschuß von Salmiak zusetzt. Hierauf wird sie bei 100º C. zur Trockne
verdampft, und der Rückstand mit einer concentrirten Salmiaklösung, welche ihm
alles Rhodium entzieht, so lange gewaschen, bis das Waschwasser nicht mehr
merklich rosenroth gefärbt ist. Die filtrirte Flüssigkeit dampft man mit einem
großen Ueberschuß von Salpetersäure ab, welche den Salmiak zerstört, und wenn
nur noch das Rhodiumsalz übrig ist, beendigt man das Abdampfen in einem
Porzellantiegel, befeuchtet den Rückstand mit ein wenig Schwefelammonium und
vermengt ihn mit seinem drei- bis vierfachen Gewicht Schwefel. Man stellt
dann den mit seinem Deckel versehenen Porzellantiegel in einen hessischen Tiegel
und füllt den Zwischenraum mit Kohlengestiebe. Das Ganze wird auf die lebhafte
Rothglühhitze gebracht, und im Tiegel bleibt metallisches Rhodium zurück,
welches man als nahezu rein betrachten kann, nachdem man es lange Zeit mit
starkem Königswasser und hernach mit concentrirter Schwefelsäure sieden
ließ.
Um dieses Rhodium in vollkommen reinen Zustand überzuführen, vermengt man es mit
seinem 3–4fachen Gewicht Zink, schmilzt es bei schwacher Rothglühhitze,
rührt gut um, läßt kurze Zeit in Ruhe und gießt dann. In dem Augenblick wo sich
die beiden Metalle legiren, entwickelt sich eine solche Hitze, daß ein Theil des
Zinks verflüchtigt werden kann; man muß alsdann den Tiegel mit der größten
Sorgfalt wieder bedecken.
Die erhaltene Legirung behandelt man mit concentrirter Salzsäure, welche viel
Zink auflöst und eine krystallisirte Masse hinterläßt, die eine Verbindung von
Zink und Rhodium im stöchiometrischem Verhältniß (RhZn²) ist. Letztere
löst man in Königswasser auf, und versetzt die Lösung mit überschüssigem
Ammoniak, bis sich der Niederschlag ganz oder doch beinahe vollständig aufgelöst
hat. Diese Flüssigkeit erhält man einige Zeit im Sieben und dampft sie dann in
geeigneter Weise ab, wodurch man das gelbe Salz erhält, welches eine Verbindung
von Rhodium, Chlor und Ammoniak (2Rh, 3 Cl, 5AzH³) ist; dasselbe läßt man
mehrmals krystallisiren; mit ein wenig Schwefel in einem Kohlentiegel bei hoher
Temperatur calcinirt, gibt es reines und zusammenhängendes Rhodium, welches man
hernach ohne Verlust mittelst des Knallgas-Löthrohrs in einer kleinen
Kapelle aus Kalk schmelzen kann.
Das Rhodium schmilzt weniger leicht als das Platin; in einem Feuer welches 300
Grm. Platin zu schmelzen gestattet, kann man in derselben Zeit nur 40 bis 50
Grm. Rhodium schmelzen. Nach unseren Beobachtungen ist dieses Metall gar nicht flüchtig: es
oxydirt sich aber schwach auf der Oberfläche, wie das Palladium. Das in
Berührung mit Kalk geschmolzene Rhodium ist frei von Silicium, einem steten
Begleiter desselben, sowie von Osmium, dessen letzte Spuren erst im stärksten
Feuer verschwinden, und es hat sehr schätzbare physische Eigenschaften erlangt.
Weniger weiß und weniger glänzend als das Silber, hat es fast denselben Ton wie
das Aluminium. Es ist dehnbar und hämmerbar, aber nur im Zustand großer
Reinheit.
Die Dichtigkeit des reinen und geschmolzenen Rhodiums ist 12,1.
5. Iridium.
Zur Darstellung desselben verwendet man Osmium-Iridium, welches man
mittelst Zink pulverisirt (siehe S. 385) und dann mit seinem fünffachen Gewicht
Baryumsuperoxyd glüht, wie es zur Bereitung des Ruthemiums (S. 385) angegeben
wurde. Die erhaltene schwarze Masse wird durch sehr lange fortgesetztes Kochen
in Königswasser von der Osmiumsäure befreit, dann versetzt man die Auflösung mit
der Quantität Schwefelsäure, welche zur Fällung des in der Flüssigkeit
vorhandenen Baryts, dessen Gewicht man kennt, genau erforderlich ist. Die
aufgelösten Chlormetalle haben eine sehr dunkle gelblichrothe Farbe; man dampft
sie ab, nachdem man einen Ueberschuß von Salzsäure zugesetzt hat, und gegen das
Ende gibt man Salmiak in Stücken hinein, so daß die Flüssigkeit gesättigt wird,
aber eine viel größere Menge davon als zum Fällen des Iridiums erforderlich ist.
Man dampft dann in einem auf 60° C. erwärmten Raum oder im Wasserbad zur
Trockne ab, und nachdem aller saure Geruch verschwunden ist, wascht man den
Rückstand mit einer concentrirten Salmiaklösung, bis die Flüssigkeit farblos
abläuft (wodurch ihm außer den dem Platin fremdartigen Metallen das Rhodium
entzogen wird), hernach mit Wasser welches etwas weniger Salmiak enthält. Auf
dem Filter bleibt das rosenrothe Rutheniumsalz von Claus und hauptsächlich Iridiumsalmiak zurück. Dieser auf dem Filter
zurückbleibende schwarze Iridiumsalmiak wird getrocknet, dann bei beginnender
Rothglühhitze calcinirt, so daß die Ammoniaksalze vollständig und die
Chlormetalle heilweise zersetzt werden. Ein Wasserstoffstrom entzieht die
letzten Spuren von Chlor oder Sauerstoff, und man erhält einen lockern
Metallschwamm, worin sich noch keine Legirung bilden konnte. Das Königswasser
zieht aus demselben manchmal ein wenig Platin aus, von welchem aber keine Spur
zurückbleibt; es entzieht ihm auch ein wenig Osmium, aber nicht alles darin
befindliche. Dieses Pulver wird in einem Gemisch von Salpeter und Kalihydrat
geschmolzen, dann sorgfältig gewaschen und in einem Kohlentiegel zum Weißglühen erhitzt, wodurch
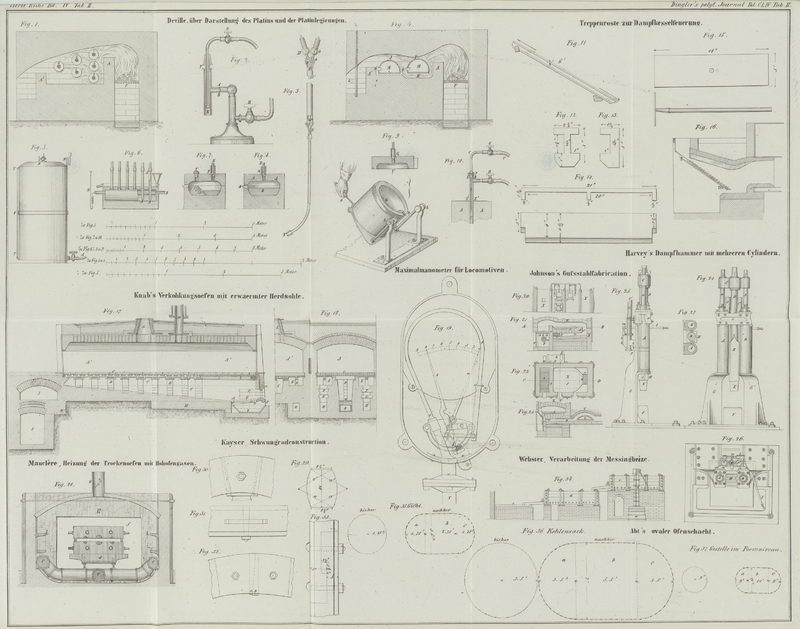
es cohärent wird, endlich in einen kleinen Kalkofen (Fig. 8 Tab. II)
gebracht, welchen man mit Sauerstoff- und reinem Wasserstoffgas speist.
Man erhitzt das Metall einige Zeit stark in einer oxydirenden Atmosphäre (um zu
ermitteln ob die Atmosphäre eine oxydirende ist, hält man ein Zündhölzchen oder
einen Eisendraht in die aus dem Ofen tretende Flamme; sie müssen darin mit
lebhaftem Funkensprühen brennen). Nachdem aller Osmiumgeruch verschwunden ist,
vergrößert man die Geschwindigkeit der beiden Gase so daß, während ihr
gegenseitiges Verhältniß beibehalten bleibt, der Sauerstoff mit dem ganzen Druck
der Gasometer, nämlich wenigstens 4–5 Centimeter Quecksilbersäule,
entweicht. Das Iridium schmilzt dann nach und nach und wird endlich so flüssig
wie Quecksilber. Um 25 Gramme Iridium zu schmelzen, braucht man, nachdem der
Ofen angeheizt ist, wenigstens 200 bis 300 Liter Sauerstoffgas und folglich
zweimal so viel Wasserstoffgas. Das Leuchtgas ist in Paris nicht so rein, daß
wir es zum Schmelzen des Iridiums hätten verwenden können.
Ein Iridiumzain ist rein weiß und polirtem Stahl etwas ähnlich, dessen Glanz er
hat. Unter dem Hammer gibt er nach, wird etwas platt und zerbricht wie ein
krystallinisches Metall. Weißglühend verhalt er sich besser unter dem Hammer;
wahrscheinlich könnte man bei dieser Temperatur und vermittelst eines Prägwerks
seine krystallinische Textur zerstören und folglich ihn schmieden, wie man es
für das Zink und gewisse Aluminiumlegirungen macht.Hr. Hulot, bei der
Pariser Münze angestellt, hat unseres Wissens zuerst dieses mechanische
Mittel angewandt, um durch das Schmelzen krystallisirte Metalle
hämmerbar zu machen, nämlich ihnen ihre Textur zu benehmen, so daß sie
bearbeitet werden können.
Das geschmolzene Iridium hat dieselbe Dichtigkeit wie das Platin, nämlich 21,15.
– Das Iridium legirt sich mit dem Zink und dem Zinn; letztere Legirung
hat zur Formel Sn²Jr.
Tafeln